C’est l’histoire d’une femme de 47 ans qui, pendant plus de dix ans, a vécu avec une maladie auto-immune réfractaire à neuf lignes de traitement. Cette anémie hémolytique auto-immune était associée à deux autres pathologies liées à un dysfonctionnement du système immunitaire : un purpura thrombopénique immunologique et le syndrome des antiphospholipides.
L’anémie hémolytique auto-immune (AHAI) résulte de la production d’anticorps qui s’attaquent aux globules rouges. Selon la température à laquelle ces anticorps réagissent – au-dessus ou au-dessous de 37 °C – on distingue les formes à « anticorps chauds » et celles à « agglutinines froides ».
Le purpura thrombopénique immunologique (PTI) est un trouble de la coagulation provoqué par une diminution du nombre de plaquettes. Dans le PTI, le système immunitaire produit des anticorps dirigés contre les plaquettes du sujet, entraînant leur destruction.
Le syndrome des antiphospholipides (SAPL) est une maladie auto-immune caractérisée par des thromboses vasculaires, en l’occurrence des caillots veineux et artériels, la persistance d’auto-anticorps dirigés contre des protéines liées aux phospholipides (principaux lipides des membranes cellulaires).
Une anémie auto-immune rebelle aux traitements
Chez cette femme, tout débute en 2014 avec une anémie hémolytique auto-immune (AHAI), résistante aux traitements, avec des agglutinines froides et, auparavant, des auto-anticorps chauds. Elle n’avait répondu à aucune des neuf thérapies successives, incluant des corticoïdes à plusieurs reprises, trois traitements successifs par rituximab (un anticorps dirigé contre l’antigène CD20 présent à la surface des lymphocytes B), des immunoglobulines intraveineuses à fortes doses (IVIG), ainsi que divers immunosuppresseurs (azathioprine, bortézomib, hydroxychloroquine, cyclophosphamide, ciclosporine A et mycophénolate mofétil).
Le rituximab, pourtant pilier du traitement de l’AHAI, s’est révélé inefficace chez cette patiente. Ce constat rejoint les données cliniques : environ un tiers des patients ne répondent pas à ce médicament et présentent des rechutes fréquentes. Ici, même une nouvelle perfusion de rituximab, cinq semaines avant la thérapie CAR-T, administrée pour gagner du temps avant la production des cellules CAR-T en laboratoire, n’a pas permis de contrôler la maladie.
Dans sa forme rebelle aux traitements, l’anémie hémolytique auto-immune est une affection potentiellement mortelle, associée à une altération majeure de la qualité de vie. Cette pathologie s’accompagne d’une hyperbilirubinémie, c’est-à-dire une concentration anormalement élevée de bilirubine dans le sang. La bilirubine est un pigment issu de la dégradation des globules rouges lors de leur destruction massive (hémolyse) par les anticorps. L’hémolyse est intense, les taux d’hémoglobine chutent, et la patiente devient dépendante des transfusions. Cette dépendance transfusionnelle expose l’organisme à une surcharge en fer et est source de complications organiques à long terme.
En 2015, l’histoire se complique : la patiente développe un syndrome des antiphospholipides, responsable de thromboses répétées qui imposent un traitement anticoagulant au long cours. Puis, en 2019, survient un purpura thrombopénique immunologique, marqué par une diminution du nombre de plaquettes.
Cette patiente est donc atteinte de trois maladies distinctes, mais qui ont comme point commun d’être liées à une dérégulation des lymphocytes B, une population de globules blancs produisant des auto-anticorps.
Au fil des années, les traitements s’enchaînent sans parvenir à contrôler durablement la maladie. Rien n’y fait, même pas le rituximab, anticorps monoclonal pourtant capable de cibler spécifiquement les lymphocytes B.
C’est alors que l’équipe de Fabian Muller de l’hôpital universitaire d’Erlangen (Allemagne) envisage une nouvelle option thérapeutique. L’état clinique de la patiente se détériore. Le taux d’hémoglobine est à 6,1 g/dL (valeurs normales chez la femme : environ 12 g/dL), la concentration de lactate déshydrogénase (LDH) dans le sang est élevée, ce qui témoigne d’une intense destruction des globules rouges. Face à cette hémolyse active, la patiente a besoin en moyenne d’une transfusion sanguine par jour, parfois davantage, jusqu’à trois concentrés de globules rouges. Aucune alternative thérapeutique efficace ne semble disponible.
Trois maladies, une même cible : les lymphocytes B exprimant CD19
C’est dans ce contexte que lui est proposée, en février 2025, une approche encore peu utilisée en cas de pathologie auto-immune : une thérapie par cellules CAR-T (CAR-T cells) dirigées contre l’antigène CD19.
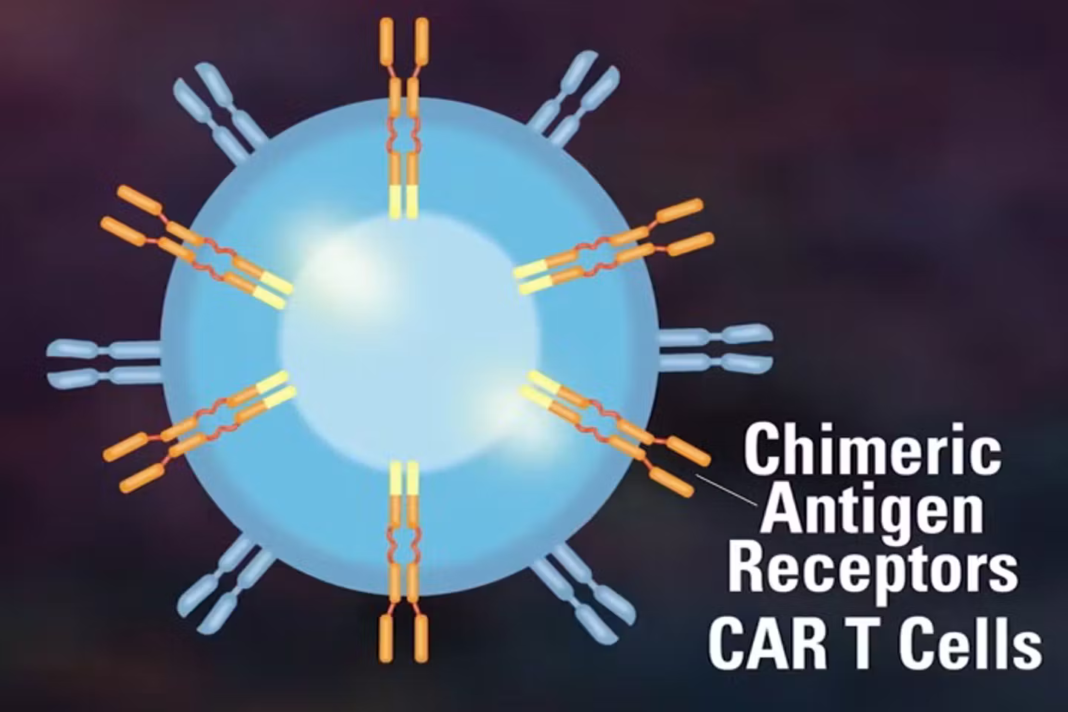
Cette technologie, appelée « cellules CAR-T » (prononcer « car-ti »), repose sur l’utilisation de lymphocytes T autologues génétiquement modifiés par un vecteur viral. Ces lymphocytes T autologues sont modifiés car ils deviennent porteurs d’un récepteur artificiel, chimérique, conçu pour se lier à un antigène, en l’occurrence le CD19. Ces lymphocytes T sont alors porteurs d’un CAR, acronyme de Chimeric Antigen Receptor (récepteur chimérique de l’antigène).
Des lymphocytes T armés d’un récepteur artificiel ciblant les lymphocytes B
La première étape pour obtenir ces lymphocytes T porteurs d’un récepteur à l’antigène chimérique (CAR-T) consiste à prélever les lymphocytes T du patient lors d’une procédure appelée leucaphérèse. Ce procédé permet de séparer et de collecter spécifiquement ces globules blancs (leucocytes), tout en réinjectant les autres composants sanguins au patient. Cette étape est cruciale pour garantir un échantillon suffisamment riche en lymphocytes T pour les manipulations ultérieures. Une fois génétiquement modifiés afin qu’ils expriment le récepteur CAR capable de reconnaître le CD19, présent à la surface des lymphocytes B, on les réinjecte au malade.
Une fois réinjectés dans l’organisme, ces lymphocytes T reprogrammés vont cibler et détruire les lymphocytes B responsables de la production des auto-anticorps.
Avant la perfusion, la patiente a reçu une chimiothérapie dite de lymphodéplétion, destinée à favoriser l’expansion in vivo des cellules CAR-T.
La patiente a reçu un million de cellules CAR-T par kilogramme de poids corporel, ce qui a rapidement entraîné une profonde diminution du nombre des lymphocytes B.
Publiées en janvier 2025 et janvier 2026 dans le Journal of Thrombosis and Haemostasis, The Lancet et The New England Journal of Medicine, des études ont montré que la thérapie CAR-T peut induire des rémissions prolongées dans le lupus érythémateux disséminé (maladie pouvant affecter de nombreux organes et notamment la peau, les reins, les articulations, les poumons et le système nerveux), la sclérodermie systémique (pathologie caractérisée par une sclérose de la peau et des organes internes, et l’atteinte de la microcirculation) et d’autres maladies auto-immunes généralisées.
Rémission totale de l’anémie hémolytique auto-immune à J25
Une semaine après la perfusion de cellules CAR-T, les transfusions deviennent inutiles. Le taux d’hémoglobine commence à remonter dès le neuvième jour et atteint des valeurs normales à J25. Les marqueurs biologiques suivent la même trajectoire : les concentrations sanguines de bilirubine et de LDH se normalisent en moins d’un mois, traduisant l’arrêt de l’hémolyse. Le taux des agglutinines froides diminue progressivement, tandis que les auto-anticorps antiphospholipides deviennent indétectables et le restent au cours du suivi de onze mois.
Parallèlement, le purpura thrombopénique immunologique (PTI) se stabilise, le taux de plaquettes augmentant graduellement. D’autres paramètres biologiques associés au PTI restent anormaux, mais sans qu’il soit nécessaire de recourir à un traitement spécifique supplémentaire. Par ailleurs, le traitement anticoagulant, initialement indispensable en raison du syndrome des antiphospholipides, est progressivement réduit de moitié, puis interrompu après dix mois, sans que ne survienne de nouvelle thrombose.
Réinitialisation du compartiment B
Un élément central de cette observation, publiée le 9 avril 2026 dans la revue Med, tient à l’effet des cellules CAR-T sur les lymphocytes B. Ceux-ci disparaissent rapidement de la circulation après le traitement, puis réapparaissent environ un an plus tard sous la forme d’une population composée à 98 % de cellules B « naïves », ce qui correspond à un véritable « reset » du compartiment B, là où le rituximab n’avait jamais réussi à reprogrammer ainsi le système immunitaire.
Autrement dit, le compartiment B a été réinitialisé en profondeur, ce qui explique la persistance de la rémission. La thérapie CAR-T a entraîné une élimination profonde et durable des lymphocytes B pathologiques auto-réactifs, dépassant largement ce que permet habituellement un traitement par rituximab.
Cette thérapie – baptisée zorpocabtagene-autoleucel (Zorpocel, en abrégé) – a permis une véritable réinitialisation du compartiment B.
Sur le plan de la tolérance, aucun des effets indésirables les plus redoutés des cellules CAR-T n’a été observé. Il n’y a eu ni syndrome de relargage des cytokines (fièvre, hypotension, insuffisance respiratoire), ni syndrome de neurotoxicité associée au traitement par cellules CAR-T. Des anomalies biologiques ont toutefois été notées (toxicité hématologique et élévation des transaminases), probablement liées à une surcharge en fer ou à la toxicité des médicaments antérieurs.
Rémission simultanée de trois maladies auto-immunes distinctes
À onze mois de suivi, cette patiente est en rémission complète, sans traitement transfusionnel. Pendant toute la période de suivi après la thérapie par cellules CAR-T, le taux d’anticorps antiphospholipides n’a jamais réaugmenté, ce qui suggère que la profonde réinitialisation (reset) des lymphocytes B a empêché leur réapparition. Ainsi, « chez cette patiente, trois maladies auto-immunes distinctes ont répondu à la thérapie par cellules CAR-T. Alors que la rémission d’un PTI, la disparition d’anticorps antiphospholipides ou l’efficacité dans une anémie hémolytique auto-immune ont déjà été rapportées séparément après une thérapie CAR-T, nous sommes les premiers à obtenir une rémission sans traitement, avec une seule perfusion de CAR-T CD19, dans un cas complexe associant trois maladies auto-immunes différentes », déclarent les médecins et chercheurs allemands.
Ces auteurs soulignent qu’il s’agit d’une observation unique, qui ne permet pas de tirer des conclusions définitives. D’où la nécessité de conduire des essais cliniques contrôlés, sur un effectif plus large et une durée de suivi plus longue, pour évaluer la place réelle de cette stratégie dans la prise en charge des maladies auto-immunes sévères et réfractaires aux traitements classiques.
Pour cette femme de 47 ans, le tournant est déjà concret : après plus de dix ans de maladie, neuf lignes de traitement et des années de transfusions quotidiennes, une seule perfusion CAR-T a suffi, à ce stade, à induire une rémission rapide et durable d’une anémie hémolytique réfractaire, à normaliser un syndrome des antiphospholipides et à stabiliser un purpura thrombopénique immunologique, le tout sans les effets secondaires les plus redoutés de cette thérapie. Dix jours après la perfusion, elle sortait de l’hôpital, ayant retrouvé « une augmentation rapide et remarquable de la force physique et une activité quotidienne normale ».
Pour en savoir plus :
Korte IK, Kharboutli S, Völkl S, et al. CD19 CAR-T therapy induces remission in refractory autoimmune hemolytic anemia with ITP and antiphospholipid syndrome. Med. 2026 Apr 9:101075. doi: 10.1016/j.medj.2026.101075
Li R, Pan H, Zhang L, et al. CD19 CAR T-Cell Therapy for Autoimmune Hemolytic Anemia. N Engl J Med. 2026 Jan 15 ;394(3) :253-267. doi : 10.1056/NEJMoa2509820
Friedberg E, Wohlfarth P, Schiefer AI, et al. Disappearance of antiphospholipid antibodies after anti-CD19 chimeric antigen receptor T-cell therapy of B-cell lymphoma in a patient with systemic lupus erythematosus and antiphospholipid syndrome. J Thromb Haemost. 2025 Jan;23(1):262-266. doi: 10.1016/j.jtha.2024.09.024
Trautmann-Grill K, von Bonin M, Georgi A, et al. Salvage treatment of multi-refractory primary immune thrombocytopenia with CD19 CAR T cells. Lancet. 2025 Jan 4 ;405(10472) :25-28. doi : 10.1016/S0140-6736(24)02504-2
Müller F, Taubmann J, Bucci L, et al. CD19 CAR T-Cell Therapy in Autoimmune Disease – A Case Series with Follow-up. N Engl J Med. 2024 Feb 22 ;390(8) :687-700. doi : 10.1056/NEJMoa2308917
Avouac J. Les CAR-T cells ont-elles leur place dans lespathologies inflammatoires et auto-immunes ? Bull Acad Natl Med. 2024 ; 208 :1036-1044. doi : 10.1016/j.banm.2024.06.018
Source:
www.lemonde.fr